برنامههای دسترسی جامع درمانی با استفاده از سلول درمانی پیشرفته
پژوهشگران امیدوارند با استفاده از برنامه دسترسی جامع (EAP) در سلولدرمانی پیشرفته به درمانهای موثر برای بیماریهای صعب العلاج برسند.
امتیاز:

به گزارش بنیان، دپارتمان های سلول درمانی اخیرا شاهد بحث چالش برانگیزی مبنی بر این موضوع که چگونه می توان فرآیند دسترسی به درمان های موجود را برای کودکان بیمار راحتر کرد هستند. از این رو پیشنهاد شده است تا یک حمایت درمانی را برای کودکان با بیماریهای صعب العلاج بوسیله سلول درمانی جایگزین کرد. همچنین این اولین باری نیست که در مورد یک برنامه دسترسی جامع که شامل درمان بالقوه تغییر دهنده زندگی کودکان بوده، بحث می شود.
از طرف دیگر طراحی مطالعات بالینی برای بکار بردن روش های سلول درمانی برای کودکان سوالاتی را به وجود آورده که پاسخ به آن ها جهت تایید این روشها ضروری می باشد. همچنین باید در نظر داشت که طبق قوانین و مقررات FDA اصطلاح برنامه دسترسی جامع صرفا جهت توصیف گروهی از بیماران بوده که در حال دریافت یک درمان بوده که به طور رسمی هنوز تایید نشده است. از این رو در مطالعات از اختصار EAP (Expanded Access Program) جهت اشاره به آن استفاده شده است. FDA و نهادهای نظارت بر سلامت عمومی در سایر کشورها همیشه مسیری برای "استفاده دلسوزانه" از درمان ها را جهت توسعه درمانی داشته اند. این قالب درمانی در دهه 1980 نمود پیدا کرد. در طول بحران ایدز، بیش از 100000 بیمار داروهای ضد رتروویروسی تحت EAPs دریافت کردند. 30 سال بعد، و تا سال 2010، FDA بیش از هزار درخواست EAP را در سال دریافت کرده که بیش از 99٪ از آنها تایید شده است. یک مطالعه نشان داد که 76٪ از داروهای موجود از طریق EAP در سال 2016 به تایید FDA رسیدند. در سال 2018، رئیس جمهور آمریکا قانونی جدید جهت درمان بیماران لاعلاج از طریق EAP تصویب کرد.
طبق ضوابط، هر دو مسیر دسترسی جامع FDA و قانون Right to try، هزینه توقف با سازنده محصول می شود. از طرف دیگر گزارش شده است که سازندگان داروئی از درخواست برای استفاده دلسوزانه (compassionate use) می ترسند، زیرا آنها را در موقعیتی بدون برد قرار می دهد. اگر آنها این درخواست را رد کنند، می تواند مورد هجمههای جریانهای اجتماعی قرار گیرد. اگر درخواست را تایید کنند و دارو را به صورت رایگان تهیه کنند نیز ممکن است از لحاظ مالی دچار ضرر و زیان شوند. از طرف دیگر اگر تولیدکنندگان داروئی درخواست را تایید کنند اما برای محصول هزینه کنند، ممکن است بازهم با موارد دیگری از مشکلات مواجه شوند. در نهایت، اگر آنها قیمت بسیار پایینی را تحت EAP دریافت کنند، و آن قیمت بعدا تغییر کند، ممکن است سازنده بعداً با مشکل مواجه شود.
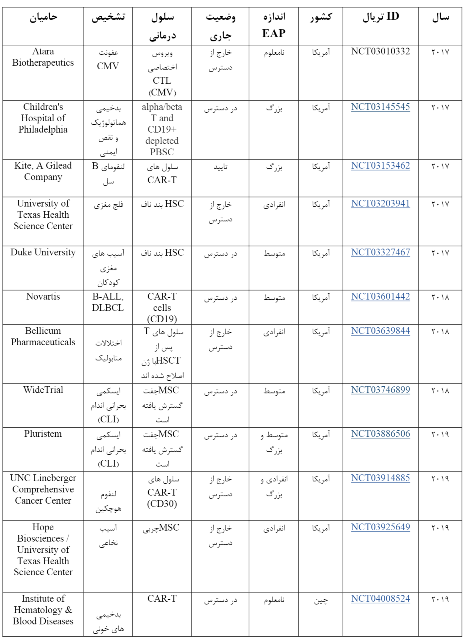
جدول زیر تمام درمانهای با EAP را نشان میدهد که از ابتدای سال 2017 تا اواسط سال 2021 در سلول درمانی پیشرفته تأیید شده اند. در این بازه زمانی 4.5 ساله، در مجموع 3471 درمان بالینی وجود دارد. کارآزماییهای سلولدرمانی پیشرفته در تمام ثبتهای جهانی فهرست شدهاند، از جمله 913 کارآزمایی ثبت شده برای انجام در ایالات متحده، اما تنها 27 تأییدیه EAP در ClinicalTrials.gov فهرست شده است. به نظر میرسد که تعداد EAP ها 3 درصد از کل تأییدیه های ایالات متحده برای داروهای جدید تحقیقاتی (IND) در سلول درمانی است، از طرفی تعدادی از این EAP در خارج از ایالات متحده است. شاید حامیان مالی در کشورهای دیگر به دنبال این مسئله باشند که با اعلام این مسئله که EAP در حال انجام مورد تایید FDA بوده به مطالعه اعتبار ببخشند.
_cm57.png)
_83py.png)
از آنجایی که تنها 27 مطالعه EAP در این جدول وجود دارد، اجرای هر گونه بررسی آماری بر روی این داده ها دشوار است. در اینجا مواردی وجود دارد که علت های این مسئله است.
سلول درمانی پیشرفته شامل 27 EAP بوده که 6 مورد از آن ها برای محصولات CAR-T (سلول تی کایمریک گیرنده آنتیژن) است. برخی داده ها قبل از تایید FDA به یک محصول CAR-T بسته شدند. برخی EAP ها نیز که در حال انجام بوده در مواردی که محصول با مشخصات تولید مطابقت نداشته، به محصولات CAR-T مورد تایید FDA نمی رسد. توزیع کارآزمایی ها بر اساس تشخیص بیش از 80٪ از 27 EAP بوده که توزیع آن ها نیز به این صورت بوده که 10 (37٪) مورد برای درمان سرطان، 8 (30٪) مورد برای شرایط عصبی، 4 (15٪) مورد برای مبارزه با بیماری های ویروسی از جمله COVID-19 اختصاص داده شده است.
مطالعات EAP از نظر اندازه در 3 دسته انفرادی، گروههای با اندازه متوسط، و جمعیتهای بزرگ تقسیم بندی می شوند. EAP برای بیماران منفرد معمولاً به هیچ وجه در ClinicalTrials.gov ثبت نمی شود، بنابراین فهرست موجود در این جدول فقط نوک کوه یخ است. برخی از حامیان این لیست بیش از یک EAP را برای کاربردهای مختلف یک محصول ثبت کردهاند، در حالی که دانشگاه دوک رویکردی سادهتر را در پیش گرفت و یک EAP را برای پوشش چندین اختلال عصبی-پیشرونده تشکیل داد. FDA الزامات گزارش دهی متفاوتی برای اندازه های مختلف EAP دارد، اما مرز بین گروه های با اندازه متوسط و بزرگ یا به وضوح تعریف نشده و یا به شدت اعمال نمی شود. حامیان این EAP ها همه شرکت های دارویی سنتی یا مؤسسات دانشگاهی نیستند. برخی از آنها به نظر سازمان هایی هستند که بانک های زیستی را با درمان های بالینی ترکیب می کنند. شرح EAP در ClinicalTrials.gov شامل هیچ گونه اطلاعات مالی نمی شود. اما حامی EAP باید یک طرح بازیابی هزینه را به FDA ارسال کند، و برای EAP هایی که اندازه متوسط یا بزرگ هستند، این طرح می تواند شامل هزینه های اداری باشد. اطلاعات موجود در پرونده IND به FDA محرمانه است. با این حال، هنگامی که یک EAP برای چند بیمار در چندین سایت راه اندازی شد، ممکن است اطلاعات هزینه توسط مدیریت یک سایت شرکت کننده درز کند. به علاوه، همیشه این امکان وجود دارد که بیماران آنچه را که پرداخت کرده اند به اشتراک بگذارند.
پایان مطلب/
لینک منبع:
1. Verter F. Parent’s Guide to Duke’s Research and Expanded Access Program of Cord Blood Therapies for Neurodevelopmental Disorders. Parent's Guide to Cord Blood Foundation Newsletter TO BE Published 2021-11-15
2. Yong J, Moffett M, Lucas S. Implementing a Global Expanded Access Program (EAP) for Infantile-Onset Spinal Muscular Atrophy (Type I): Understanding the Imperative, Impact and Challenges. J Neuromuscular Diseases 2019; 6(2):227-231.
3. Kiefer P, Kirschner J, Pechmann A, Langer T. Experiences of caregivers of children with spinal muscular atrophy participating in the expanded access program for nusinersen: a longitudinal qualitative study. J Rare Diseases 2020; 15:194
4. Yates N. I have spinal muscular atrophy. Critics of the $2 million new gene therapy are missing the point. STATnews Published 2019-05-31
5. Code of Federal Regulations. Charging for investigational drugs under an IND. 21CFR312.8 Updated 2020-04-01
6. FDA. Charging for Investigational Drugs Under an IND - Questions and Answers. Guidance for Industry Published 2016-06
7. FDA. An Overview of FDA's Expanded Access Process and the New Individual Patient Expanded Access Application. DDI Webinar Accessed 2021-11-01
8. Amorosa A, Tebas P. Is It Time to Rethink the Expanded-Access Programs for HIV Infection? J. Infectious Diseases 2007: 196:974–977.
9. Moch KI. Ethical Crossroads: Expanded Access, Patient Advocacy, and the #SaveJosh Social Media Campaign. MA@PoC 2017; 1(1):e119-e130.
10. Miller JE, Ross JS, Moch KI, Caplan AL. Characterizing expanded access and compassionate use programs for experimental drugs. BMC Research Notes 2017; 10:350.
11. Right-to-Try. What is Right to Try? righttotry.org Accessed 2021-11-01
12. Walker S. Expanded Access Versus Right-to-Try. Hospital Pharmacy 2020; 55(2):79-81.
13. Miseta E. Now That Right To Try Is Law, What Does It Mean To You? Clinical Leader Published 2018-11-29
14. Merlan A. A Controversial Autism Treatment Is About to Become a Very Big Business. VICE Published 2021-10-06